Porque é que a água molha? A ciência explica como as moléculas interagem ao entrar em contacto com uma superfície
Descubra como a química molecular e a temperatura interagem para criar a sensação de humidade que sentimos diariamente ao entrar em contacto com a água.

Caminhar sob um céu cinzento e ser surpreendido por uma chuva repentina é uma experiência comum que todos já vivemos alguma vez na vida. Nesse instante, a roupa começa inevitavelmente a absorver a água, transformando a leveza das peças num fardo pesado colado ao corpo. Esta transformação obedece a leis físicas que ditam o comportamento da matéria líquida.
Não é preciso ser um especialista dedicado a estudar os segredos do clima e da dinâmica atmosférica para saber que a água é protagonista da física terrestre. Não importa se falamos de uma grande tempestade ou da humidade contida no ar de uma floresta, o comportamento hídrico é constante. A chave reside na interação das partículas minúsculas com os objetos que as rodeiam no dia a dia.
O segredo da adesão e da polaridade molecular: porque é que a água molha?
O conceito de molhado manifesta-se quando o fluido se espalha por uma superfície em vez de se manter como uma esfera fechada. Notará que o tecido escurece e adere à pele devido a uma propriedade química chamada adesão forte. As moléculas de água sentem uma ligação poderosa por outros corpos, procurando estabelecer um contacto físico com os materiais circundantes que é difícil de quebrar sem aplicar calor.
¿Por qué el agua moja? #MiSeñal tiene la respuesta. #LaCienciaCuenta pic.twitter.com/OCLer8WCbp
— Señal Colombia (@SenalColombia) November 3, 2016
Cada uma das partículas que compõem uma gota funciona de forma semelhante a um íman microscópico com extremidades carregadas de eletricidade. Possuem uma zona com carga negativa e outra com carga positiva, o que as torna elementos muito reativos face ao seu ambiente imediato. Materiais comuns como o vidro ou as fibras de uma camisa apresentam esta natureza elétrica polarizada. Ao entrarem em contacto, as cargas opostas atraem-se intensamente.
Esta forte atração mútua é responsável pelo facto de o fluido se deslocar pelos poros da matéria com uma facilidade surpreendente e se espalhar. Ao contrário do mercúrio, cujas partículas preferem permanecer unidas entre si formando bolas isoladas, o H2O procura a companhia externa. A sensação de estar encharcado depende do tempo que o líquido consegue manter-se ligado à superfície cutânea. Se não se agarrassem assim, a chuva escorregaria.
Arrefecimento por evaporação e a razão física da sensação de frio
Após o contacto com o líquido, sentimos uma descida brusca da nossa temperatura corporal, especialmente na zona afetada. Este fenómeno de arrefecimento requer uma transferência de energia específica para que as moléculas mudem de estado físico. Para que as partículas abandonem o estado líquido e se transformem em gás, precisam de se separar das suas vizinhas através deste processo energético natural.
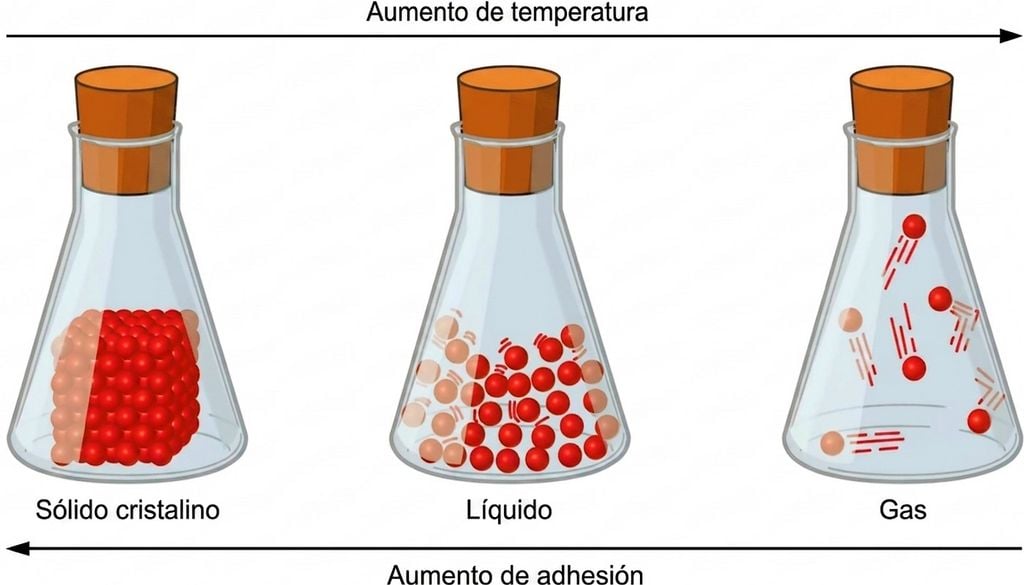
O calor necessário para esta transformação é extraído diretamente do ambiente mais próximo, que, no caso da roupa húmida, é a nossa própria pele. É esta perda de energia térmica que gera o arrepio característico que sentimos, mesmo em dias em que o sol brilha. O nosso sistema nervoso associa tanto esta relação térmica que, por vezes, confundimos a baixa temperatura com a presença de líquido real. Tocar em algo gelado pode dar-nos essa impressão.
Esta capacidade de absorver calor é uma ferramenta muito útil que a física utiliza para equilibrar condições na vida quotidiana. Observamo-lo claramente ao aplicar álcool sobre uma ferida, sentindo um frescor instantâneo porque esse produto evapora-se com grande rapidez. Da mesma forma, o mecanismo da transpiração depende desta troca de energia para arrefecer o nosso organismo e evitar sobreaquecimentos prejudiciais à saúde.
Humidade atmosférica e o paradoxo do vapor de água no fogo
Existe um tipo de humidade que não conseguimos ver a olho nu, mas que influencia a forma como percebemos o ambiente. O ar funciona como um recipiente limitado que só pode conter uma quantidade máxima de vapor de água em suspensão. Quando este limite é atingido, o processo de evaporação dos líquidos pára, fazendo com que nos sintamos desconfortáveis e pegajosos, mesmo sem estar a chover diretamente sobre nós.

A capacidade de armazenamento da atmosfera varia consoante a temperatura indicada pelo termómetro em cada momento. Enquanto as massas de ar quentes conseguem reter grandes volumes de vapor sem chegar à saturação, as zonas frias atingem esse estado com facilidade. Por este motivo, os recantos escuros de uma casa apresentam frequentemente um ambiente com um nível de humidade muito mais elevado. Ao não receber calor, o líquido não consegue transformar-se em gás.
É fascinante que, em situações de calor extremo, como as que se verificam em torno de um grande incêndio florestal, sejam libertadas imensas nuvens de vapor. Embora associemos as chamas à secura absoluta, a combustão gera uma grande quantidade de vapor de água que se eleva em direção ao ar quente. Como o ambiente está a uma temperatura elevada, este vapor não forma gotas visíveis, permitindo que a roupa seque rapidamente.
Não perca as últimas notícias da Meteored e desfrute de todo o nosso conteúdo no Google Discover totalmente GRÁTIS
+ Siga a Meteored